温州医科大学宋增强课题组JMC | 新型抗骨质疏松候选药物β-三氟乙氧基二甲基硒醚的发现
英文原题:Design, Synthesis, and Biological Evaluation of β-Trifluoroethoxydimethyl Selenides as Potent Antiosteoporosis Agents

通讯作者:宋增强(温州医科大学)、黄盛斌(温州医科大学附属口腔医院)、薛伟伟(重庆大学)
作者:Yao Wu, Bin Li, Linkun Ying, Yao Chen, Yuxin Zhang, Chaoming Hu, Yichi Zhang, Lele Yi, Weiwei Xue*, Shengbin Huang*, and Zengqiang Song*
骨质疏松症(osteoporosis,OP)是一种以骨量降低和骨组织微结构破坏为特征,导致骨脆性增加和易于骨折的代谢性骨病,其具有很高的致死率并产生承重的经济负担。研究报告显示,全球约有 2 亿人患有骨质疏松症,每年将近 900 万人发生骨质疏松性骨折。破骨细胞调节的骨吸收与成骨细胞调节的骨形成之间的平衡对维持正常的骨骼结构具有至关重要的作用。当骨吸收超过骨形成,骨重塑被破坏,进而导致骨质疏松。因此,通过使用药物抑制破骨细胞形成、促进成骨细胞形成,被认为是治疗骨质疏松症最有效的策略之一。现有的治疗骨质疏松的大多数药物为抑制骨吸收类药物,目前报道的抑制骨吸收并促进骨形成的药物绝大多数为蛋白类药物,存在不良反应、疗效低等缺陷。因此,研发新的治疗骨质疏松的药物具有非常迫切的需求。
该研究采用分子杂交策略,设计了新型β-三氟乙氧基二甲基硒醚类化合物。发展了温和条件下直接、高效合成该类化合物的新方法,并合成了一系列β-三氟乙氧基二甲基硒醚。通过测试合成化合物抑制破骨细胞分化活性及构效关系研究,发现化合物4aa活性最佳。接下来作者进一步考察了化合物4aa体内抑制破骨细胞的活性和作用机制。结果表明,化合物4aa可有效抑制破骨细胞分化(图1A)、破骨细胞形成及骨吸收。同时,化合物4aa可有效抑制破骨细胞相关基因的表达,并通过抑制MAPK 和 NF-κB 信号通路抑制破骨细胞分化。此外,化合物4aa可有效促进成骨细胞形成(图1B,C),并通过激活BMP2 信号通路促进成骨细胞分化。体内活性测试结果表明,化合物4aa可有效抑制去卵巢骨质疏松小鼠体内骨流失(图2)。表面等离子体共振结果表明化合物4aa有可能靶向RANKL蛋白。
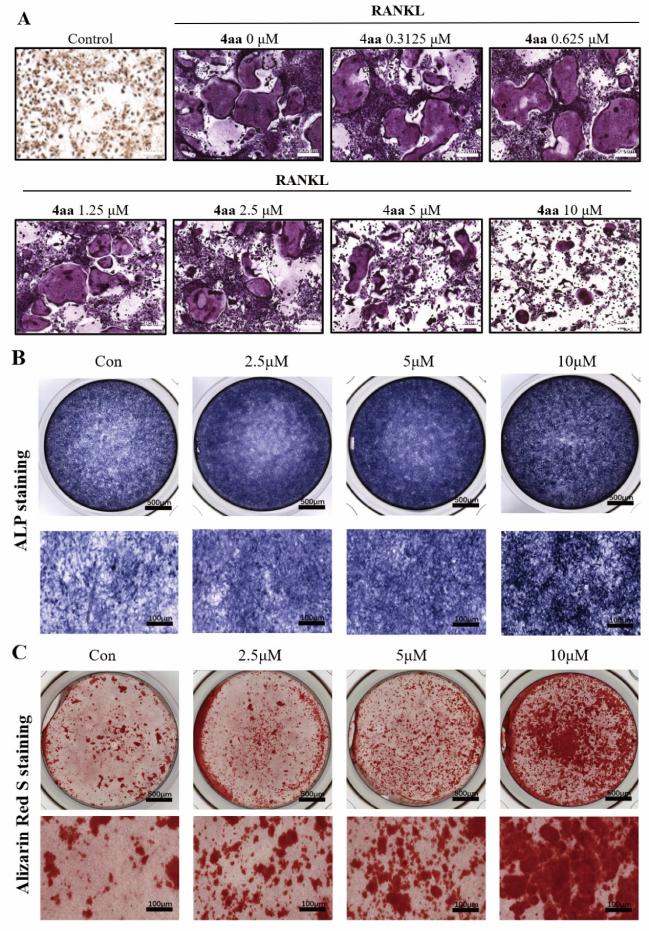
图1. 化合物4aa抑制破骨细胞分化、促进成骨细胞形成。图片来源:J. Med. Chem.

图2. 化合物4aa抑制去卵巢骨质疏松小鼠体内骨流失。图片来源:J. Med. Chem.
综上所述,温州医科大学药学院宋增强课题组设计并合成了一系列新型β-三氟乙氧基二甲基硒醚类化合物,通过体内外活性测试,发现了通过抑制破骨细胞分化、促进成骨细胞形成阻止骨流失的新型抗骨质疏松候选药物。该研究成果发表在药物化学领域顶级期刊Journal of Medicinal Chemistry 上。温州医科大学硕士研究生吴瑶、博士研究生李宾和硕士研究生应林锟为该论文的共同第一作者,重庆大学薛伟伟副教授、温州医科大学附属口腔医院黄盛斌教授和温州医科大学宋增强副研究员为该论文的共同通讯作者。本工作得到了国家自然科学基金、浙江省自然科学基金和温州市科协的资助。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Yao Wu, Bin Li, Linkun Ying, Yao Chen, Yuxin Zhang, Chaoming Hu, Yichi Zhang, Lele Yi, Weiwei Xue*, Shengbin Huang*, and Zengqiang Song*
J. Med. Chem. 2024, 67, 9, 7585–7602
Publication Date: April 17, 2024
https://doi.org/10.1021/acs.jmedchem.4c00438
© 2024 American Chemical Society
宋增强副研究员简介
宋增强,温州医科大学药学院副研究员,博士生导师。研究领域为骨细胞相关疾病(骨质疏松、骨关节炎、骨瘤等)的新药研究。以第一作者或通讯作者在J Med Chem、Eur J Med Chem、Org Lett等期刊发表学术论文10余篇,申请多项国家发明专利,主持并参与国家自然科学基金、浙江省自然科学基金等多项课题。
https://www.x-mol.com/university/faculty/164563
(本稿件来自ACS Publications)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!
































 京公网安备 11010802027423号
京公网安备 11010802027423号