Nat. Catal.:镍/光协同催化烯烃的双碳官能团化反应
长期以来,从廉价易得的碳氢化合物出发,高效构建高价值手性分子仍然是合成化学家面临的一项重要挑战,这是因为与大多数官能团相比C(sp3)-H键反应性较低,而且,同时精确控制多个非等价C(sp3)-H键的化学、区域和立体选择性难度颇大。近年来,光催化氢原子转移(HAT)策略已广泛应用于C(sp3)-H键的直接官能团化,例如:化学家利用四丁基铵十钨酸盐(TBADT)和二芳基酮高区域选择性地裂解电性和空间可及的C(sp3)-H键,并将其转化为C-C、C-O、C-N、C-F和C-S键等。另一方面,光催化三组分自由基烯烃双官能团化反应可以快速高效构建复杂分子,这是因为其可以利用一次操作在π体系中同时安装两个新的官能团。然而,参与此类转化的开壳自由基中间体的高反应性和不稳定性会导致新生成立体中心的对映选择性控制极具挑战性。此外,尽管HAT和过渡金属的协同催化已被用于C(sp3)-H键的对映选择性芳基化、烷基化、烯基化、酰化和氰化(图1a),但是直接活化C(sp3)-H键来实现烯烃的不对称双官能团化尚待发展,这主要存在以下两方面挑战:1)手性配体必须克服竞争性双组分副反应,并且在三组分过程中有效实现新立体中心的绝对立体控制;2)溶剂和/或偶联试剂中易于活化的C-H键无竞争性活化,以此避免反应过程中的效率和选择性。
近日,瑞士苏黎世大学的Cristina Nevado教授(点击查看介绍)课题组将光催化氢原子转移(HAT)与镍催化相结合,高区域选择性、化学选择性和对映选择性地实现了三组分烯烃的双官能团化(图1b),从而制备了一系列高价值手性α-芳基/烯基羰基/膦酸酯和1,1-二芳基烷烃化合物。值得一提的是,该方法不仅条件温和、底物范围广、原子经济性高,而且还能实现生物活性分子的后期修饰以及药物相关分子的合成。相关成果发表在Nature Catalysis 上。
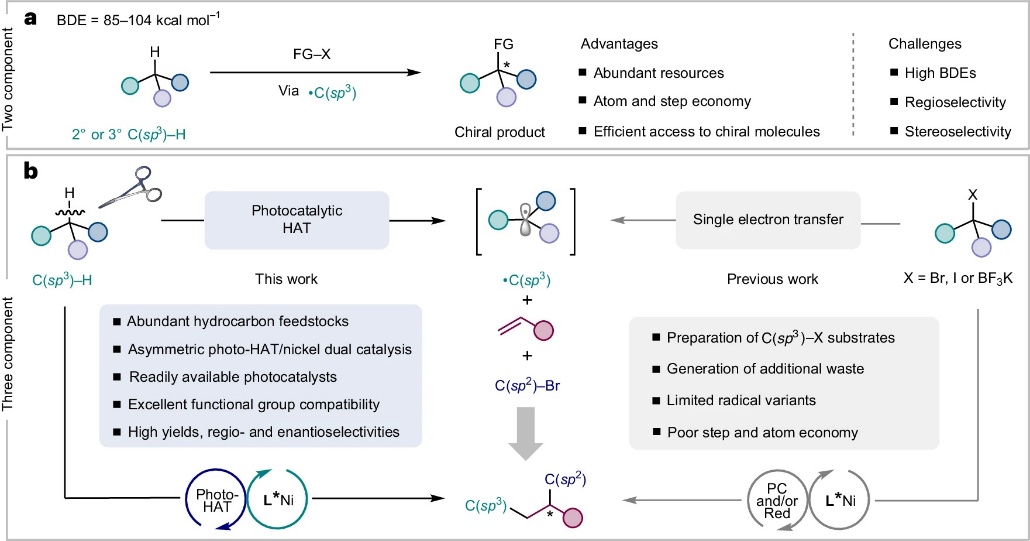
图1. 背景介绍。图片来源:Nat. Catal.
首先,作者选择环己烷、丙烯酸叔丁酯和4-溴苯腈为模板底物对反应条件进行筛选(图2),并获得最佳条件:即三种底物在TBADT(2 mol%)为HAT催化剂、NiBr2•DME(10 mol%)为金属催化剂、手性BiIm L1(15 mol%)为配体、磷酸钾(K3PO4,2 equiv)为碱、丙酮/三氟甲苯(PhCF3)为混合溶剂的条件下于5℃进行紫外光照射,能以80%的产率和96:4 e.r.值获得(R)-2-(4-氰基苯基)-3-环己基丙酸叔丁酯1,同时通过X-射线衍射分析证实其绝对构型。此外,对照实验表明光催化剂、镍、配体和光照至关重要,并且手性BiIm模板的电性和空间性质对反应效率(L1-L5)有显著影响。类似地,当使用异丙醇作为自由基前体时,在二芳基酮PC I为HAT催化剂、NiBr2•DME、L5和Na2CO3的存在下进行光照时,可以85%的产率和96:4 e.r.值获得所需的三组分偶联产物2。

图2. 反应条件筛选。图片来源:Nat. Catal.
在最优条件下,作者对芳基/烯基溴化物的底物适用性进行了考察(图3),结果显示对位不同基团取代的芳基溴化物(1、3-15)、邻氟/间氟芳基溴化物以及2,4-、3,4-和3,5-二取代芳基溴化物(18-23)、多环芳基溴化物(24-28)、杂芳基溴化物(29-38)、烯基溴化物(39、40)甚至天然产物衍生的芳基溴化物(如:D-葡萄糖(41)、雌酮(42)、(-)-薄荷醇(43)、胆固醇(44)和(+)-α-生育酚(45))均能兼容该反应,以良好的产率和优异的对映选择性获得相应产物,尽管对位含有强供电子基团的芳基卤化物(如:4-溴苯甲醚(16)和4-溴硫代苯甲醚(17))需要增加光照强度来获得相应的双官能团化产物。值得一提的是,该方法还能合成非甾体抗炎药(NSAIDs)衍生物(如:氟苯布洛芬(27)和萘普生(28)),而且含有氯原子的芳基溴化物进行反应时表现出优异的化学选择性(9、19、21、23、35)。在某些情况下,特别是对于富电子(杂)芳基和烯基溴化物,使用L5作为手性配体并稀释反应可提高产率和对映选择性。
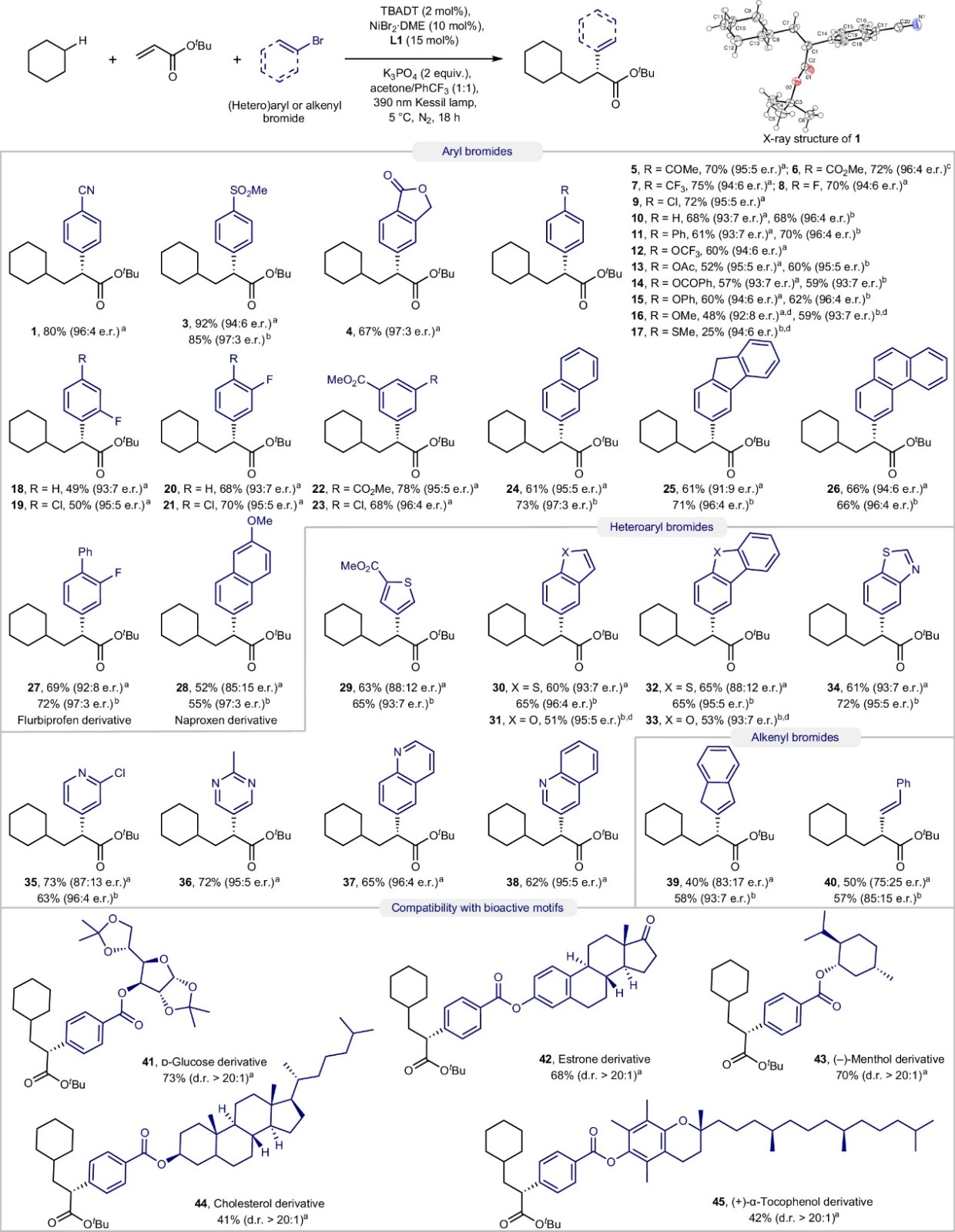
图3. 底物拓展一。图片来源:Nat. Catal.
接下来,作者考察了C-H键前体的底物范围(图4),结果显示各种环尺寸的环烷烃(如:环戊烷(46)、环庚烷(47)、环辛烷(48)和环十二烷(49))、2,3-二甲基丁烷(50)、带有不同吸电子基团的烃衍生物(51-55)、2,3-二甲基-2-丁醇(56)、含醚烷烃衍生物(57、58)均能以良好的产率、优异的区域和对映选择性进行烯烃双官能团化反应,其中2,3-二甲基丁烷(50)在二级C-H键上被选择性活化(因为一级C-H键的高键解离能)。然而,甲基叔丁基醚、甲苯和Boc-保护的吡咯烷却无法参与三组分反应,而是获得双组分芳基-烷基交叉偶联产物。此外,作者发现当二苯甲酮衍生物PC I在改进的反应条件下用作光催化剂时,异丙醇(2)、3-戊醇(59)和环戊基甲醚(60)也可顺利实现这一转化。其次,作者探索了烯烃的底物适用性,结果显示带有不同取代基的丙烯酸酯(61-66)、乙烯基膦酸酯(67、68)、α,β-不饱和酮(69)、丙烯酰胺(70)以及含有不同官能团的苯乙烯(71-75)均能兼容该反应,以良好的产率和对映选择性获得双官能团化产物。

图4. 底物拓展二。图片来源:Nat. Catal.
为了展示该方法的实用性,作者对产物进行了衍生化,具体而言:1)α-芳基酯3通过酸性水解和酯化或酰胺化过程,以良好的产率(66-82%)和高非对映选择性(>20:1 d.r.)获得L-酪氨酸和L-色氨酸衍生物(76-77),进而表明该方法在快速构建复杂氨基酸衍生物方面具有潜力;2)α-芳基酯3在LiAlH4的作用下进行还原得到醇78(97:3 e.r.),再通过亲核取代以高产率和对映选择性转化为相应的β-芳基溴化物79、β-芳基酰胺80和β-芳基硫醇81(图5a)。如图5b所示,市售环戊烷、丙烯酸叔丁酯和4-溴-2-氯-1-(甲基磺酰基)苯进行三组分交叉偶联反应以65%的产率和97:3 e.r.值获得产物82,随后经三氟乙酸水解和2-氨基吡嗪酰胺化获得Piragliatin先导化合物83(产率:72%,e.r.值:97:3),极大地简化了先前的合成步骤。类似地,通过使用上述三步合成序列,作者还成功地合成了对映体富集的葡萄糖激酶激活剂RO28-1675(85,97:3 e.r.)。
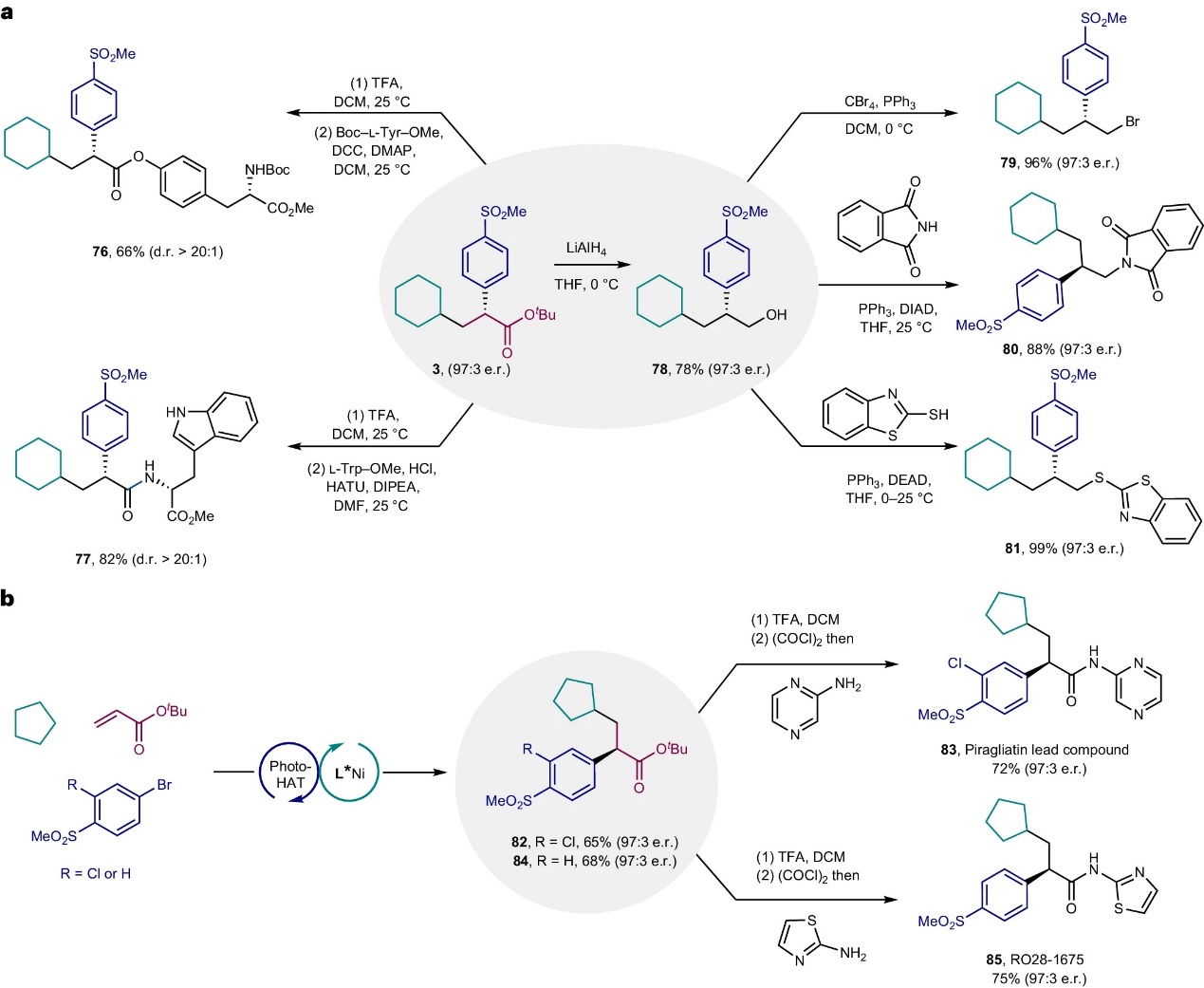
图5. 合成应用。图片来源:Nat. Catal.
为了进一步探究反应机理,作者进行了一系列实验,具体而言:1)向标准条件下加入TEMPO后会完全抑制所需的烷基芳基化反应(图6a),并且高分辨质谱(HR-MS)检测到混合物中的TEMPO加合物86和87,进而证明该反应存在烷基自由基中间体;2)环丙基烯烃在标准条件下进行自由基钟实验以20%的产率获得产物89(图6b),其通过顺序自由基加成、开环和芳基化过程进行;3)对照实验排除了产物去消旋作用或自由基对双键的Giese型加成,然后进行对映选择性α-芳基化过程;4)预合成的4-CF3C6H4Ni(II)L1Br配合物90无法催化该反应,这主要是由于90在无芳基溴的情况下不稳定并且具有很强的可见光吸收特性。相比之下,在芳基溴存在下使用10 mol%配合物90作为催化剂进行反应时能以67%的产率和95:5 e.r.值获得产物7(图6c),这些结果表明芳基-Ni(II)络合物可能不是催化循环中的主要中间体;5)激光闪光光解实验表明在环己烷存在下TBADT*明显衰减且遵循线性Stern-Volmer方程(双分子速率常数k=3.14 × 107 M−1 s−1),而丙烯酸叔丁酯和4-溴苯甲腈却无法猝灭TBADT*(图6d),这说明环己烷被光催化剂的激发态活化并形成碳自由基,与图6a、b中的自由基捕获和自由基钟实验相一致。
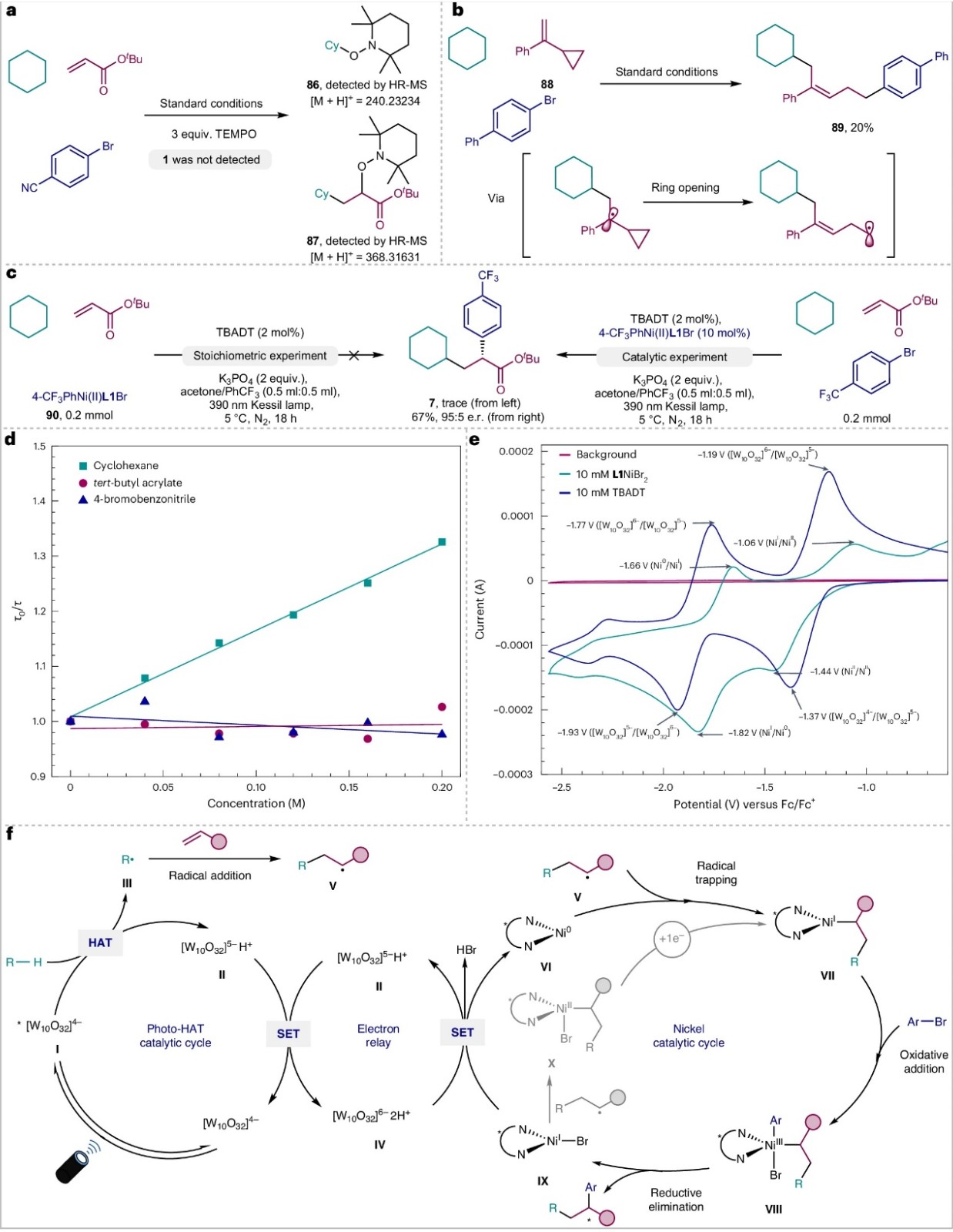
图6. 机理研究。图片来源:Nat. Catal.
在此基础上,作者提出了可能的反应机理(图6f):首先,十钨酸四-N-丁基铵在光激发下生成激发态十钨酸四-N-丁基铵I,I从C(sp3)-H键亲核试剂中攫取氢原子并生成单还原十钨酸盐II和碳中心自由基III,随后II发生歧化反应获得双还原十钨酸盐IV并再生基态TBADT。与此同时,III与烯烃发生自由基加成获得加合物V,其可被Ni(0)物种VI捕获并获得烷基-Ni(I)中间体VII,VII与芳基溴化物发生氧化加成获得烷基-Ni(III)-芳基中间体VIII,接着经还原消除便可得到所需的双碳官能化产物以及Ni(I)物种IX。最后,IX和双还原TBADT IV进行单电子转移再生Ni(0)催化剂VI和单还原TBADT II以完成催化循环,并且这一过程得到循环伏安法的支持(图6e),因为[W10O32]5–/[W10O32]6-的还原电位比NiI/Ni0更低。此外,NiI/NiII/NiIII催化序列也有可能(图6f,灰色),即Ni(I)物种IX与自由基加合物V进行加成得到烷基-Ni(II)中间体X,X通过单电子还原得到Ni(I)物种VII。
总结
Cristina Nevado教授研究团队以十钨酸盐或二芳基酮与手性联咪唑啉 (BiIm) -镍配合物作为组合催化剂,高区域选择性、化学选择性和对映选择性地实现了三组分烯烃的双官能团化反应,进而制备了一系列高价值手性α-芳基/烯基羰基/膦酸酯和1,1-二芳基烷烃化合物。此外,该方法不仅条件温和、底物范围广、原子经济性高,而且还能实现生物活性分子的后期修饰以及药物相关分子的合成,进而为通过C(sp3)-H键活化实现更多不对称多组分反应提供了一种新思路。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Nickel-catalysed enantioselective alkene dicarbofunctionalization enabled by photochemical aliphatic C–H bond activation
Xia Hu, Iván Cheng-Sánchez, Wangqing Kong, Gary A. Molander, Cristina Nevado
Nat. Catal., 2024. DOI: 10.1038/s41929-024-01153-0
导师介绍
Cristina Nevado
https://www.x-mol.com/university/faculty/44772
(本文由吡哆醛供稿)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!
































 京公网安备 11010802027423号
京公网安备 11010802027423号